I. Tổng quan vềESMOHướng dẫn năm 2025
Tháng 8 năm 2025, ESMO chính thức công bố Hướng dẫn thực hành lâm sàng của ESMO về chẩn đoán, điều trị và theo dõi ung thư phổi không tế bào nhỏ giai đoạn sớm và tiến triển tại chỗ, được đăng tải trên tạp chí ung thư hàng đầu Annals of Oncology. Đây là bản cập nhật toàn diện đầu tiên kể từ phiên bản năm 2017 và cung cấp tài liệu tham khảo cực kỳ đáng tin cậy cho các bác sĩ ung thư trên toàn thế giới.

Ung thư phổi có tỷ lệ mắc và tử vong cao nhất trong tất cả các loại ung thư trên toàn cầu. Mỗi năm, có hơn 2,2 triệu trường hợp mắc mới và hơn 1,8 triệu ca tử vong, khiến ung thư phổi trở thành nguyên nhân hàng đầu gây tử vong do ung thư ở cả nam và nữ. Ung thư phổi không tế bào nhỏ (NSCLC) chiếm khoảng 80-85% tổng số bệnh nhân ung thư phổi. Trong bối cảnh nghiêm trọng này, việc ban hành hướng dẫn năm 2025 đã tạo động lực khoa học mới cho thực tiễn lâm sàng, với việc cập nhật các chiến lược xét nghiệm dấu ấn sinh học đặc biệt quan trọng.
II. Giải thích các cập nhật hướng dẫn quan trọng
2.1 Xét nghiệm dấu ấn sinh học: Từ “tùy chọn” đến “thiết yếu”
Hướng dẫn năm 2025 đánh dấu một bước điều chỉnh chiến lược quan trọng liên quan đến xét nghiệm dấu ấn sinh học. Hướng dẫn này nêu rõ rằng xét nghiệm dấu ấn sinh học là cần thiết cho việc đưa ra quyết định điều trị ở bệnh nhân mắc ung thư phổi không tế bào nhỏ giai đoạn IB-III.
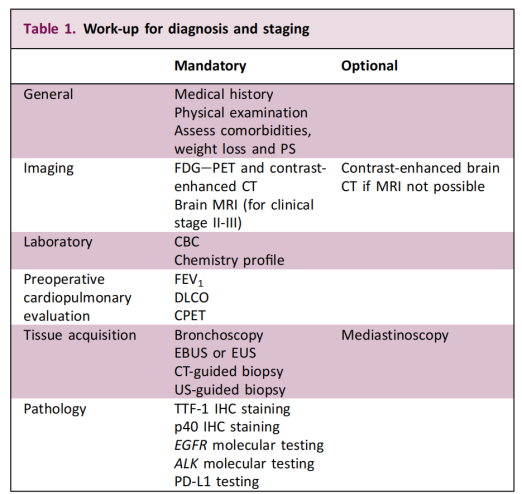
Khuyến nghị này mở rộng phạm vi xét nghiệm phân tử từ trọng tâm trước đây chỉ dành cho bệnh nhân mắc bệnh giai đoạn nặng sang các trường hợp giai đoạn sớm, có thể phẫu thuật cắt bỏ. Mục tiêu cốt lõi là xác định các đột biến gen chủ đạo và cung cấp cơ sở khoa học cho điều trị chính xác cá nhân hóa. Hướng dẫn này cũng nhấn mạnh rằng tính khả thi của sinh thiết và phương pháp chẩn đoán nên được xác định bởi một nhóm đa ngành dựa trên đặc điểm của bệnh nhân và khối u.
Về chiến lược xét nghiệm cụ thể, hướng dẫn khuyến nghị rõ ràng rằng xét nghiệm gen nên được thực hiện trước khi đưa ra quyết định phẫu thuật, và ít nhất phải bao gồm EGFR và ALK. Khái niệm “xét nghiệm trước” này có ý nghĩa lâm sàng sâu sắc đối với việc phân loại chính xác và điều trị cá nhân hóa ung thư phổi không tế bào nhỏ giai đoạn sớm – tính kịp thời và chính xác của kết quả xét nghiệm quyết định trực tiếp lựa chọn liệu pháp bổ trợ tiếp theo.
2.2 Những đột phá trong điều trị ung thư phổi không tế bào nhỏ giai đoạn sớm có mang gen gây ung thư chủ đạo
Hướng dẫn năm 2025 tích hợp bằng chứng từ nhiều nghiên cứu lâm sàng lớn để thiết lập một lộ trình điều trị chính xác rõ ràng cho bệnh nhân mắc ung thư phổi không tế bào nhỏ giai đoạn sớm có đột biến gen gây ung thư.
Bệnh nhân dương tính với đột biến EGFR:Dựa trên thử nghiệm ADAURA mang tính bước ngoặt, điều trị bổ trợ bằng osimertinib sau phẫu thuật trong ba năm đã trở thành tiêu chuẩn điều trị toàn cầu cho bệnh nhân mắc đột biến mất đoạn exon 19 hoặc đột biến L858R exon 21 của gen EGFR. Thử nghiệm ADAURA là một nghiên cứu pha III quốc tế, đa trung tâm, ngẫu nhiên, có đối chứng, đánh giá hiệu quả và độ an toàn của điều trị bổ trợ bằng osimertinib ở bệnh nhân ung thư phổi không tế bào nhỏ (NSCLC) giai đoạn IB-IIIA có đột biến EGFR đã được phẫu thuật cắt bỏ hoàn toàn. Nghiên cứu cho thấy osimertinib cải thiện đáng kể cả thời gian sống không bệnh và thời gian sống thêm toàn diện so với giả dược, thiết lập osimertinib như là tiêu chuẩn điều trị mới cho nhóm bệnh nhân này. Tuy nhiên, các phân tích thăm dò của thử nghiệm ADAURA chỉ ra rằng khoảng 36% trường hợp ngừng điều trị sớm là do tác dụng phụ và 31% là do quyết định của bệnh nhân. Phát hiện này nhấn mạnh sự cần thiết phải xét nghiệm cơ bản chính xác trước khi điều trị để đảm bảo rằng liệu pháp nhắm mục tiêu được áp dụng cho những bệnh nhân có thể thu được lợi ích bền vững.
Bệnh nhân dương tính với ALK:Dựa trên kết quả thử nghiệm ALINA, điều trị bổ trợ bằng alectinib sau phẫu thuật trong hai năm hiện nay là phác đồ chuẩn. Trong phân tích chính của thử nghiệm ALINA pha III ngẫu nhiên, nhãn mở, alectinib cho thấy lợi ích rõ rệt về thời gian sống không bệnh tái phát ở nhóm bệnh nhân giai đoạn II-IIIA, với tỷ lệ nguy cơ là 0,24. Dữ liệu cập nhật từ thử nghiệm ALINA được trình bày tại hội nghị ESMO 2025 cho thấy sau ≥3 năm theo dõi, lợi ích về thời gian sống không bệnh tái phát của alectinib vẫn “được duy trì và có ý nghĩa lâm sàng”, với tỷ lệ nguy cơ là 0,36 ở nhóm bệnh nhân giai đoạn II-IIIA. Tỷ lệ sống sót chung sau 4 năm được báo cáo gần đây nhất đạt 98,4%, tỷ lệ sống không bệnh tái phát sau 4 năm là 75,5%, và tỷ lệ sống không bệnh tái phát ở hệ thần kinh trung ương cũng được cải thiện, không có tín hiệu an toàn mới nào. Những dữ liệu mạnh mẽ này càng khẳng định alectinib bổ trợ là phác đồ chuẩn sau phẫu thuật cắt bỏ ung thư phổi không tế bào nhỏ ALK dương tính và nhấn mạnh giá trị của việc xét nghiệm chính xác để xác định những bệnh nhân này.
Lựa chọn phương pháp thử nghiệm:Hướng dẫn ESMO năm 2025 nêu rõ điều này.Xét nghiệm RT-PCR đa kênhCùng với NGS dựa trên RNA, IHC và FISH, đây là một trong những phương pháp kỹ thuật được khuyến nghị để phát hiện đột biến gen ALK. Điều này cho thấy yêu cầu cốt lõi của hướng dẫn là thực hiện xét nghiệm để hướng dẫn các quyết định lâm sàng, chứ không phải bắt buộc một nền tảng xét nghiệm cụ thể. Đối với các sản phẩm RT-PCR tập trung vào phát hiện EGFR và ALK, chiến lược xét nghiệm linh hoạt này cung cấp cơ sở lý luận vững chắc dựa trên hướng dẫn cho việc sử dụng chúng trong thực hành lâm sàng.
III. Giải pháp kỹ thuật kiểm tra độ chính xác
Hướng dẫn năm 2025 đưa việc xét nghiệm lên giai đoạn ra quyết định trước phẫu thuật, điều này nâng cao tiêu chuẩn về độ chính xác, độ nhạy và khả năng tiếp cận của xét nghiệm. Hai sản phẩm phát hiện dựa trên RT-PCR được mô tả dưới đây hoàn toàn phù hợp với các yêu cầu của hướng dẫn về mặt kỹ thuật.
3.1 Bộ dụng cụ phát hiện đột biến EGFR – Nền tảng công nghệ ARMS nâng cao
Công nghệ cốt lõiCông nghệ ARMS được cải tiến cho phép khuếch đại đặc hiệu các trình tự đột biến có số lượng thấp trên nền trình tự kiểu hoang dã cao.
Ba biện pháp bảo vệ kỹ thuật:
-ARMS được nâng cấp → cải thiện khả năng nhận diện đột biến
- Làm giàu bằng enzyme → phân giải nền kiểu hoang dã và làm giàu các trình tự đột biến
- Chặn nhiệt độ → ngăn chặn sự khuếch đại không đặc hiệu
Hiệu suấtĐộ nhạy củaTần suất alen đột biến 1%
Kiểm soát ô nhiễm: Hệ thống kiểm soát nội bộ tích hợp + enzyme UNG ngăn ngừa ô nhiễm
Thời gian hoàn thành: Hoạt động trong ống kín, xấp xỉ120 phút
Khả năng tương thích mẫu:Mô/sinh thiết dịch thểcác mẫu → giải quyết yêu cầu “kiểm thử trước”
Phạm vi phủ sóng:45 đột biếntrong các exon 18-21 của EGFR, khớp chính xác với các vùng được nhấn mạnh trong hướng dẫn (đột biến mất đoạn exon 19 và đột biến L858R ở exon 21)
Sử dụng lâm sàngHướng dẫn trực tiếp liệu pháp EGFR-TKI
3.2 Bộ kit phát hiện đột biến hợp nhất MMT EML4-ALK – Giải pháp phát hiện đột biến hợp nhất dựa trên RNA

-Nền tảng công nghệRT-PCR dựa trên RNA – mang lại những ưu điểm vượt trội so với các phương pháp dựa trên DNA trong phát hiện đột biến hợp nhất.
-Ưu điểm dựa trên RNA: Phát hiện trực tiếp các bản sao RNA lai được biểu hiện, giúp tránh hiệu quả tình trạng âm tính giả.
-Bằng chứng nghiên cứuĐối với các đột biến gen ALK có số lượng thấp, xét nghiệm RT-PCR cho kết quả chính xác hơn đáng kể so với các xét nghiệm dựa trên DNA.
-Độ nhạy: Phát hiện các sự kết hợp nhỏ nhất20 bản sao mỗi phản ứng
-Phạm vi bao phủ của các biến thể: Bao gồm12 biến thể hợp nhất EML4-ALK phổ biến(bao gồm biến thể 1 ~33%; biến thể 3a/3b cộng lại ~29%)
-Vận hành và kiểm soát ô nhiễm: Thí nghiệm trong ống kín, khoảng 120 phút; hệ thống kiểm soát quy trình tích hợp + enzyme UNG giúp ngăn ngừa kết quả sai lệch.
-Khả năng tương thích của thiết bịTương thích với nhiều thiết bị PCR thời gian thực thông dụng.
-Tuân thủ hướng dẫnHoàn toàn phù hợp với hướng dẫn của ESMO.
IV. Tính nhất quán giữa các xét nghiệm và các khuyến nghị trong hướng dẫn
Hai sản phẩm phát hiện này có độ nhất quán cao với hướng dẫn ESMO 2025 về ung thư phổi không tế bào nhỏ giai đoạn sớm và tiến triển tại chỗ ở các khía cạnh chính sau:
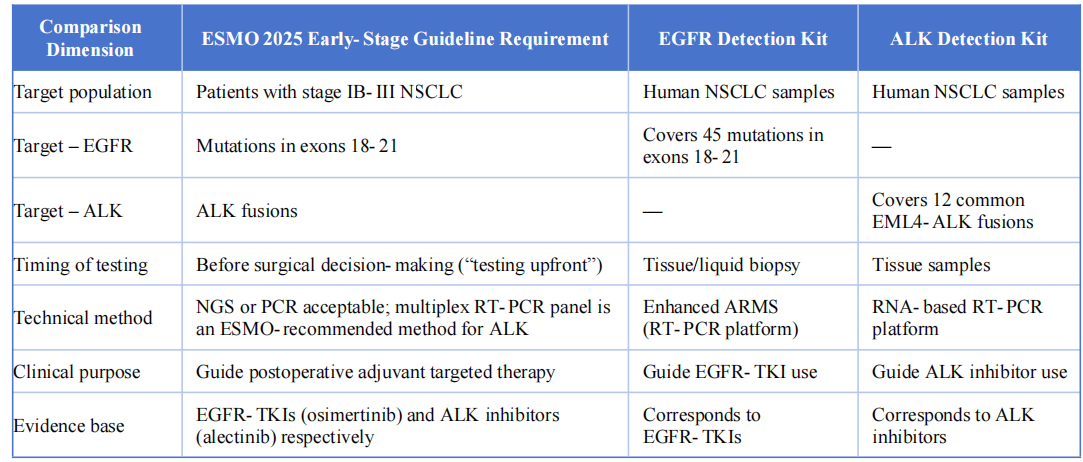
V. Kết luận
Hướng dẫn ESMO 2025 về ung thư phổi không tế bào nhỏ giai đoạn sớm mở ra một kỷ nguyên mới về chẩn đoán và điều trị chính xác, tập trung vào “Kiểm tra kỹ lưỡng ngay từ đầu, nhắm mục tiêu chính xác và tối ưu hóa điều trị.“Bộ kit phát hiện đột biến EGFR và bộ kit phát hiện hợp nhất MMT EML4-ALK đáp ứng các yêu cầu của hướng dẫn về mục tiêu, thời gian và độ chính xác thông qua các quy trình kỹ thuật riêng biệt.”
Bộ kit EGFR sử dụng công nghệ ARMS cải tiến để phát hiện các đột biến mục tiêu với độ nhạy cao trong các mẫu hạn chế, hỗ trợ cả sinh thiết mô và sinh thiết dịch để cho phép "xét nghiệm ngay từ đầu".
Bộ kit ALK dựa trên phương pháp RT-PCR dựa trên RNA, mang lại nhiều ưu điểm so với các phương pháp dựa trên DNA trong phát hiện đột biến hợp nhất, phù hợp với khuyến nghị của ESMO về việc sử dụng bảng RT-PCR đa kênh cho xét nghiệm ALK.
Sự kết hợp của hai sản phẩm này tạo thành một giải pháp xét nghiệm chính xác tuân thủ hướng dẫn ESMO 2025, hỗ trợ liệu pháp bổ trợ cá nhân hóa cho bệnh ung thư phổi không tế bào nhỏ giai đoạn sớm.
Tài liệu tham khảo:
- Zer A, Ahn MJ, Barlesi F, et al. Ung thư phổi không tế bào nhỏ giai đoạn sớm và tiến triển tại chỗ: Hướng dẫn thực hành lâm sàng của ESMO về chẩn đoán, điều trị và theo dõi. Ann Oncol. 2025;36(11):1245-1262. doi:10.1016/j.annonc.2025.08.003
Thời gian đăng bài: 06/05/2026

